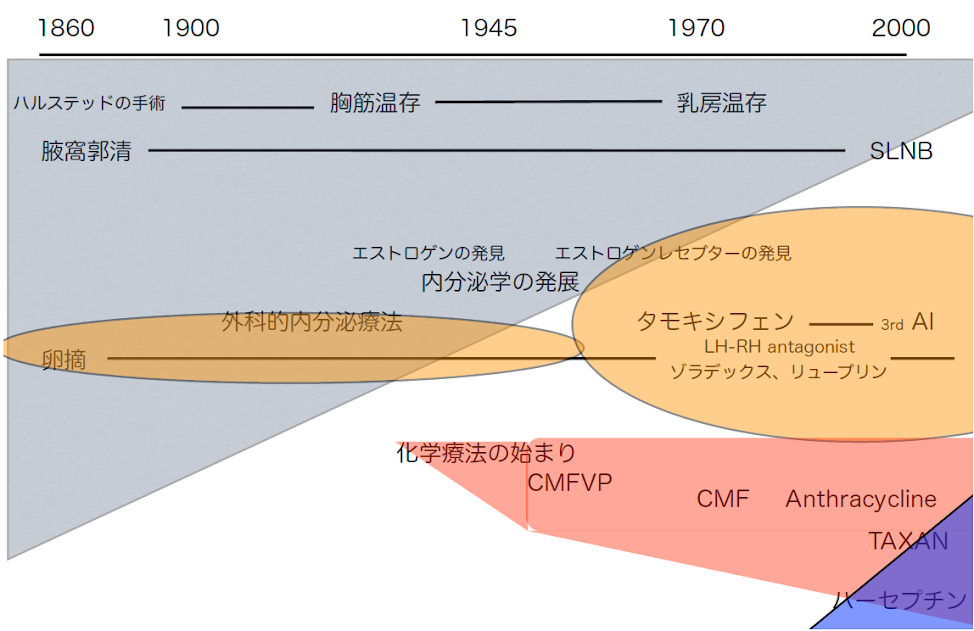
原発乳がん治療の歴史1
略語の説明、解説
ハルステッドの手術
1860年代にDr.Halstedらが提唱した術式。乳房、大胸筋、小胸筋、腋窩リンパ節を一塊にして切除する手術方法。100年近く標準手術であったため” 定型的乳房切断術”とも呼ばれた。
胸筋温存手術
大胸筋のみを温存するPatey(ペイティ、パティ)法、大胸筋も小胸筋も温存する Auchincloss(オーチンクロス、オッケンクロス)法。いずれの方法もハルステッドの術後に見られる皮膚の下にあばら骨が浮いて見えるような状況は改善した。現在の乳房切除術はAuchincloss法と同じである。
乳房温存手術(別名:乳房部分切除術)
腫瘍の周囲に正常乳腺をつけて切除する方法。切除の形から円状切除、楔状切除がある。
腋窩郭清
脇の下を走る血管神経を温存しつつ、脇の下のリンパ節を全て切除すること。Axと略される。
SLNB(Sentinel Lymph Node Biopsy:センチネル(リンパ節)生検、見張りリンパ節生検)
ラジオアイソトープ(RI法)、色素(色素法)のどちらかもしくは両方を乳房内に注射してリンパの流れに乗せ、そのRIもしくは色素が集まった腋窩リンパ節のことをセンチネルリンパ節と呼ぶ。センチネルリンパ節はがん細胞が最初に転移するリンパ節と考えられるため、手術時にセンチネルリンパ節を切除して、術中に転移の有無を病理学的に調べ(病理の先生が顕微鏡でみて調べる)て 、転移があれば腋窩郭清を行い、転移がなければ腋窩郭清を省略する方法
卵摘(正式名称は卵巣摘出術)
1860年頃、英国のDr.Beatsonが進行乳がんの患者さんの卵巣を切除することで乳がんが縮小した例があったことを報告し、以後、乳がんの治療法の一つとなった。
外科的内分泌療法
卵巣摘出術が有効であったが、その後再増大した患者さんには、別の女性ホルモンの前駆物質を産生する両側副腎切除を、さらには、ホルモン産生を促す刺激ホルモンを産生する脳下垂体切除を行った。これらを一括して外科的内分泌療法という。しかし、副腎切除や、下垂体切除は目的としている女性ホルモン以外のホルモンも低下してしまうため、それらの欠乏症状のコントロールが難しくあまり行われなかった。
エストロゲン(別名:卵胞ホルモン)
卵巣から分泌される女性ホルモンの一つ。もう一つの女性ホルモンはプロゲステロン(黄体ホルモン)
エストロゲンレセプター(別名:エストロゲン受容体(略称:ER))
エストロゲンが働くためには、細胞にある受容体(エストロゲンを鍵とすれば鍵穴)にエストロゲンが結合することが必要であることがわかった。1950年代に発見された。
LH-RH agonist(日本語訳:黄体ホルモン刺激ホルモン類似薬)
女性の月経周期は黄体ホルモンと卵胞ホルモンが周期的に増減するこことで発現しているが、LH-RH agonistを投与すると黄体ホルモン刺激が持続し、子宮は黄体期の状態で月経周期が停止し、以後卵巣からの女性ホルモン産生が止まる。卵巣摘出とほぼ同等の効果がある。薬品名:ゾラデックス、リュープリン
タモキシフェン(商品名:ノルバデックス、略称:TAM)
SERM(選択的エストロゲン受容体作動薬)と呼ばれる群に含まれる抗エストロゲン剤。エストロゲンレセプターに対してエストロゲンと競合的に結合することで、エストロゲンがレセプターに結合して作用を発揮することを止める。1981年から使えるようになった古い薬なのでたくさんのジェネリック薬(タスオミン、ソシゲン、タモキシフェン等)が存在する。
3rd AI(正式名称:第3世代アロマターゼ阻害剤、商品名:アリミデックス、フェマーラ、アロマシン)
女性ホルモンが作られる最終段階で働く酵素(アロマターゼ)の働きを止めることで女性ホルモンの血中濃度を下げる薬。
第一世代(Aminoglutetimide:日本未発売)第二世代 (Fadrozole:アフェマ:日本のみで発売)に比べて選択性が高くなって副作用が減った。
CMFVP
世界で初めて乳がんの術後治療薬として臨床試験が行われた治療法。C:Cyclophosphamide(シクロフォスファミド、略称:CPA), M:Methotrexate(メソトレキセート、メトトレキセート), F:5-FU(ファイブ-エフユー)、V:Vincristin(ビンクリスチン), P:Predonizolone(プレドニゾロン)の組み合わせ
CMF
CMFVPと治療効果がかわらないのでVPが省略された治療法。術後化学療法(CMF)群と術後無治療群の比較試験がイタリアで行われ、術後化学療法の有効性が世界で初めて証明された治療法。1970年代から欧米では乳癌術後の標準治療の一つになったが、日本ではMethotrexateの乳がんへの保険適応がなかったため長い間使えず、使えるようになったのは、なんと20年後の1996年6月。
Anthracycline(読み方:アンスラサイクリン)
Doxsorubicin(アドリアシン)Epirubicin(ファルモルビシン)等の総称。レジメンとしてはCyclophosphamide(C:エンドキサン), 5-FU(F:ファイブエフユー)と併用して、AC, CAF, EC, FECがあり、これらの治療を総称してAnthracycline containing regimen(アンスラサイクリンを含む治療法)と呼ばれる。この4種類のレジメンの治療効果、副作用は基本的には差はないと考えてられている。アンスラサイクリンを含む治療法の治療効果はCMFとの比較試験で再発を抑える力が強いことが証明され、現在の乳癌術前、術後治療の主役のひとつになっている。
主な副作用は、脱毛、嘔気嘔吐、白血球減少と抗がん剤の3大副作用が揃っている。ただし、嘔気嘔吐の頻度は制吐剤が進歩したので現在ではかなり減少してきている。また白血球減少も、白血球(正確には好中球)を増やす注射が開発され、白血球減少の伴う発熱を抑えることができるようになっている。脱毛については現在でもwig(鬘、カツラ)での対応が必要。稀だが重篤な副作用として、心毒性(心臓の働きを低下させる)と白血病がある、特に前者は容量依存性(使った量が増えるほど副作用の頻度が増える)なので、総投与量に注意する。総投与量がアドリアシンで750mg/m2, ファルモルビシンで1000mg/ m2を越すと心毒性の頻度が上昇する。通常の術前術後のAnthracyclineの投与量は、アドリアシン(ACの場合,60x4mg=240mg/ m2、CAFの場合,60×6=360mg/ m2), ファルモルビシン(ECで90×4=360mg/ m2, FECの場合,90×6=540mg/ m2)なので、不必要に心毒性を心配する量ではないが、心臓がもともと悪い人は注意が必要。転移再発の治療などでAnthracyclineが有効で、規定量以上を投与したい場合は心機能を検査しながら慎重に投与する。(※mg/ m2:身長、体重から計算した体表面積あたりの投与量のことで、日本人であれば平均的な体表面積は1.5 m2程度)
Taxan(読み方:タキサン)
いちいの木から抽出した成分から開発された化学療法剤であるPaclitaxel(パクリタキセル;昔はタキソールと呼ばれた)、Docetaxel(ドセタキセル;昔はタキソテールと呼ばれた)の総称。(※タキソール、タキソテールの呼称は間違いやすい名称のため、医療安全の観点から使われなくなった)
パクリタキセル(Paclitaxel, 略称:PTX)
太平洋いちいの木の樹皮から抽出した成分、開発当初は化学的に合成できず製薬会社はいちいの木を植林して生産したというエピソードがあるが現在は化学的に完全に合成されている。日本で使えるようになったのは19971年10月。
AC->PTX(AC4コース後パクリタキセルを4コース投与する方法)がAC単独より優ったことから、現在でも乳がんの術前術後に使われる標準的な治療法の一つ。当初PTXは3週間に1回の投与法であったが、その後投与量を3分割して毎週投与する方法が行われ、毎週法(毎週投与する方法)の方が副作用も少なく、治療効果が大きいことがわかり、現在は毎週法が主流。主な副作用は脱毛と末梢神経障害。パクリタキセルによる末梢神経障害は治療終了後もなかなか治らないことが多いため、末梢神経障害がひどくなる前に投与を中止する必要がある。また薬剤の性質上、点滴内にアルコールを含むため、アルコールにアレルギーがある人、アルコールに弱い人は注意が必要。吐き気等の副作用は少ない 。
ドセタキセル(Docetaxel;略称:DTX)
ヨーロッパいちいの木の針葉から抽出した成分。日本で使えるようになったのは1997年6月。投与法は3週間に一度の投与。FEC->DTX(FEC 4コース後ドセタキセルを4コース行う)がFECに優ったことから、これも現在の乳がん術前術後の標準的な治療法の一つ。副作用は脱毛、全身倦怠感、骨髄抑制、末梢神経障害、浮腫などで、投与中の副作用はパクリタキセルより強く辛いが、パクリタキセルのように治療終了後も続く副作用はあまりない。
ハーセプチン
細胞膜表面のHer2(ハーツー)タンパクが過剰発現している患者さん (全乳がんの約1/4)に対する治療薬(抗Her2治療薬)で、最初にできた薬。Her2タンパクに特異的に結合する抗体。通常は化学療法剤と併用して用いられる。副作用は初回投与時に起きる悪寒、発熱(インフュージョン リアクション)と心毒性(頻度は低く、可逆性)で、それ以外の副作用はほとんどない。
原発乳がん治療の歴史2

略語の説明、解説
手術
全摘
乳房切除術と同じ意味
全摘+再建
乳房切除後にインプラントを留置する一次一期再建。乳房切除後にエキスパンダーを留置し、後日インプラントに入れ替える一次二期再建が保険診療で行えるようになった。再建手術が可能になると同時に、全摘の代わりに皮下乳腺全摘(乳輪乳頭を含めた皮膚も温存し、皮下の層で乳腺のみを全てくり抜く手術)も広まってきた。
SLNB:
n(+)
当初はセンチネルリンパ節に転移が認められた場合(n+ と表現)は全例腋窩郭清を行なっていた
N(-)非郭清
センチネルリンパ節に転移がなければ腋窩郭清は省略できて、患側のリンパ浮腫が低減する。センチネルリンパ節の転移を調べる方法には通常の病理検査で調べる方法と、OSNA法と呼ばれる生化学的に調べる方法がある
微小転移(2mm以下)
2mm以下の転移は微小転移(n(mic))と呼び、微小転移症例の予後はリンパ節転移のない症例(n0)と変わらないことがわかったため、センチネルリンパ節転移が2mm以下の場合は腋窩郭清を省略できるようになった
2個以下
米国での臨床試験で、乳房温存手術で術後温存乳房に放射線をかける治療を予定している場合、センチネルリンパ節転移が2個までであれば、郭清をしてもしなくても予後は変わらないという結果が出て、そのように米国でのガイドラインの記載が2016年に変わった。
内分泌療法
閉経前
21世紀初めまではTAM(ノルバデックス、タスオミン、タモキシフェン等)を術後5年間内服する治療が標準で、LH-RHa(ゾラデックス、リュープリン)を加えるか加えないかは主治医の判断で決められ、そこに明確な基準はなかった。
LH-RHaを加えるか?
2015年 術後TAM単独群とTAM+LH-RHa群を比較した臨床試験の結果が出た。その結果、両群間に治療効果に差はなく、LH-RHaを加えた群の方が更年期障害様の副作用は強かったことから、原則はTAM 単独が推奨された。ただし、術後に化学療法を行った群で、月経が再開した人ではLH-RHaを追加した方が成績がよかったので、化学療法を行っても閉経しなかった人、化学療法で一時閉経したが、月経が再開した人ではLH-RHaを加えることが勧められた。(投与期間は術後5年間)
閉経後
20世紀末に行われた臨床試験から、閉経後の術後補助内分泌療法は、AI(アロマターゼ阻害剤:アリミデックス、フェマーラ、アロマシン)5年内服もしくは、TAM2-3年内服後AIに切り替えてTotal 5年内服するのがbestで、AI剤が服用できない場合はTAM 5年で代用するという治療が推奨されていた。その後、臨床試験は行われなかったが、TAM2-3年内服後AIに切り替えた場合、AIを5年間内服して、Total7−8年間治療する方法も容認されるようになった。2005年にTAM5年内服後にAIをさらに5年内服した方が晩期の再発を抑制できることがわかった。
化学療法
n+ or n(-) high risk
21世紀初めまでは、n(+)(=腋窩リンパ節転移陽性という意味)、もしくは、n(-) high risk(腋窩リンパ節転移はないが転移再発のリスクの高いという意味)の患者さんが化学療法の対象と考えられていた。high riskとする因子は腫瘤径が大きい、組織学的グレードが高いなど。
Subtype
乳がんは大きく4つに分類されることがわかり、4つのsubtypeに応じて術後補助療法が行われてくるようになった。ルミナル Aに分類されるとリンパ節転移があっても数が少なければ化学療法は省略されるようになった。Subtypeについての詳細は化学の授業で。
Anthra.
Anthracyclineの略語
Taxan
前項に解説あり。Paclitaxel(パクリタキセル)、Docetaxel(ドセタキセル)の総称
Anthra->Taxan
現在も乳がん術後化学療法の主流。Anthracyclineを含むレジメン(AC,EC,CAF,FEC)を3週間毎4コース施行後、Taxan(パクリタキセルもしくはドセタキセル)を12週投与する方法。パクリタキセルは毎週法で12週間投与、ドセタキセルは3週間毎4コース投与する。AC vs AC->Paclitaxel, FEC vs FEC->Docetaxel、いずれもTaxanを加えた方が再発を減らすことができた。パクリタキセルとドセタキセルのどちらが良いかの比較試験の結果は同等であった。
TAC
ドセタキセル+アドリアシン+エンドキサンの組み合わせ。CAFとの比較試験でより転移再発を抑えたが、アドリアシンとドセタキセルを同時に使うので、副作用は強い。
TC
ドセタキセル+エンドキサンの組み合わせ。ACとの比較試験でAC より再発を抑える力があることが証明された。
Dose dense AC->PTX
白血球を増やす薬(G—CSF)をあらかじめ投与しておくと、白血球が2週間で回復するのでAC, PTXを2週間隔で投与する方法。従来の3週間に1回の投与法との比較試験で転移再発を減らすことができた。日本ではG-CSFの保険適応の問題でこの投与法はできなかったが、最近、長時間作用型のG-CSFが承認されて、この投与法を検討する施設がではじめている。
分子標的治療
ハーセプチン
日本では2001年に転移再発乳がんに対して保険承認され、2008年に術後補助療法として使えるようになり、2011年に術前治療として使えるようになった。
Anthra.->Taxan+H
Anthracyclineを含むレジメン(AC,EC,FEC,CAF)4コース後、Taxan(パクリタキセルもしくはドセタキセル)とハーセプチン(H:3週毎)を4コース行い、その後ハーセプチン単独治療を通算で一年間投与する治療法。現在の標準的な治療法。術前治療として行う場合は、Anthracycline->Taxan+ ハーセプチンまでを術前に行い、ハーセプチン単独は術後に行う。
Anthra. or T ->H
Anthracycline もしくはTaxanを含む化学療法を単独で行った後でハーセプチンを1年間投与する方法。HELLA試験と呼ばれる方法で証明された投与法だが、現在では、前者が用いられることが多い。
TCbH
ドセタキセル+カルボプラチン+ハーセプチンの3剤で6コース治療後、ハーセプチン単独を通算一年間投与する方法。Anthracyclineを使わないことが特徴。
心臓が悪くてAnthracyclineが使いづらい場合、過去にAnthracuclineを使用していて今回使えない場合等に使われる治療法。副作用は前述の方法(Anthra->Taxan+H)より若干強い。2011年に保険承認された。
付記
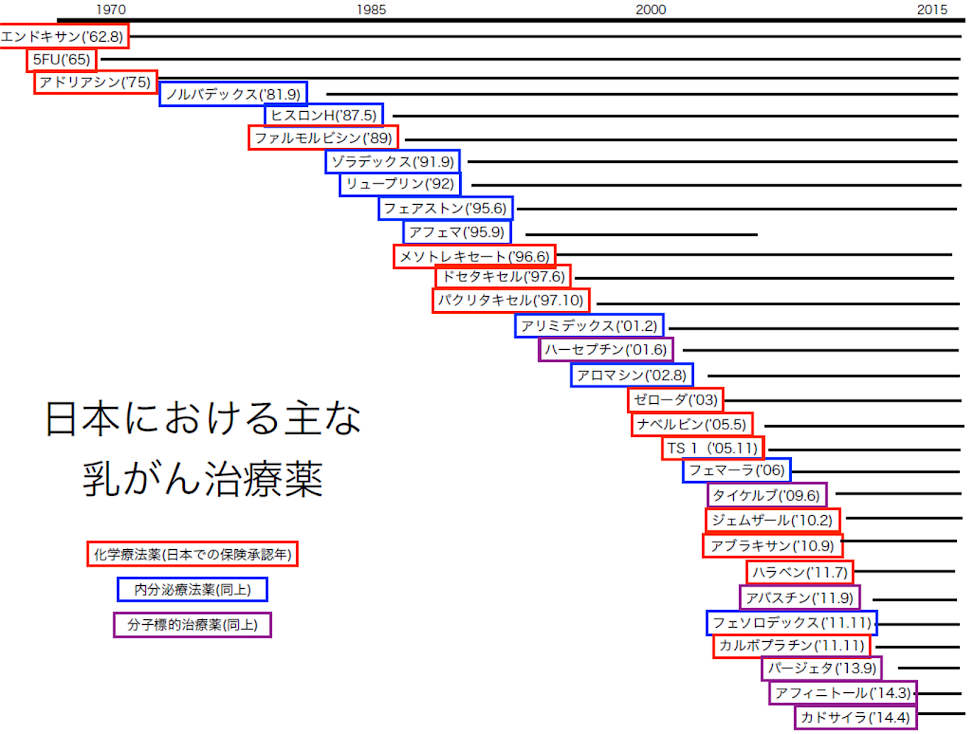
今までの歴史は、原発乳がんの治療に関する歴史です。再発乳がんの治療については複雑になるので省略しました。その代わりに、乳がん治療薬を、日本で使えるようになった年月順に並べた一覧表を作りました。皆さんが使っている(た)お薬はいつ頃から使えるようになった薬なのか参考にしていただければ幸いです。
文責:清水 哲
日本における主な乳がん治療薬